
암이나 치매 같은 질병의 시작점인 단 한 개의 세포 속 유전 설계도를 마치 3차원 입체 지도처럼 정밀하게 읽어내는 기술이 나왔다.
KAIST 생명과학과 정인경 교수팀이 미국 듀크대와 공동연구로 은 단일 세포 수준에서 유전자 발현(전사체), 후성유전체, 게놈 3차 구조를 동시에 분석하는 초정밀 분자지도 해독 기술 ‘scHiCAR’를 세계 최초로 구현했다.
이번 성과는 질병 시작점인 단일 세포의 변화를 정밀하게 관찰하지 못했던 기존 한계를 극복할 수 있어 복잡한 질환 연구에 새로운 전기를 제공할 것으로 기대된다.
하나의 세포로 질병 원인 규명
세포 상태를 결정하는 유전자는 단순히 켜고 꺼지는 스위치 이상으로, 유전자의 작동 여부와 조절 원리, 공간구조가 복합적으로 작용한다.
기존 연구는 수천~수만 개 세포 평균값을 분석해 특정 세포에서 발생하는 질병 초기 신호를 포착하기 어렵고, 각각 다른 세포에서 따로 얻은 정보를 다시 맞춰야 해서 미세한 왜곡이나 누락이 발생했다.
이에 연구팀은 전사체, 후성유전체, 3차 게놈 구조 등 이 세 가지 유전 정보를 단일 세포에서 동시에 분석하는 통합 정밀 분석 기술인 ‘트라이모달 멀티오믹스(trimodal Trimodal Multi-omics)’ 기술을 구현하고 인공지능(AI) 분석을 접목해 정확도와 재현성을 크게 높였다.
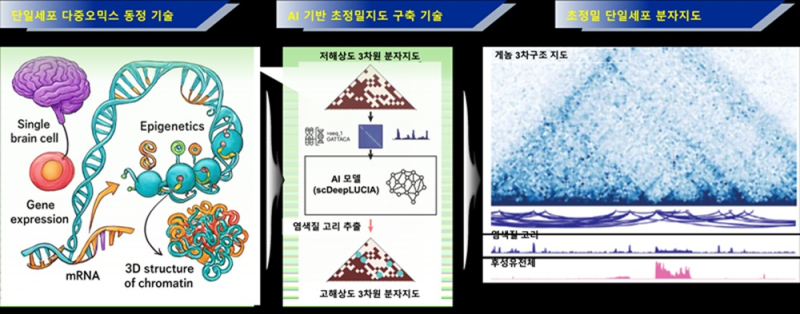
그 결과 세포 내부 유전 정보를 하나의 입체 지도처럼 읽을 수 있는 통합 분석 플랫폼을 완성했다.
연구팀은 우선 세포핵을 준비해 후성유전체와 게놈 3차 구조를 표지하고, 조합 바코딩 기술을 적용했다.
이는 여러 단계 바코드를 조합해 실험 한 번으로 수백만 개 고유 세포 식별자를 생성하는 방식이다.
이후 차세대 염기서열 분석법으로 단일 세포 특이적 정보를 통합했다.
특히 AI 분석 기술로 게놈 3차 구조 분석에 필요한 방대한 분자 정보 추출 한계를 극복했다. AI는 조직 내 극소량 존재하는 세포 아형까지 정확하게 식별하도록 돕고, 세포 한 개당 분석 비용을 약 50원(0.04달러) 수준으로 크게 낮췄다.
연구팀은 기술 실효성을 증명하기 위해 생쥐 뇌 조직 내 160만 개 세포를 대상으로 고해상도 분자지도를 구축했다.
그 결과 뇌 조직을 구성하는 22개 주요 세포 유형에서 나타나는 서로 다른 유전자 작동 원리를 확인했다.
또 근육 재생 과정에 이 기술을 적용해 근육 줄기세포가 재생될 때 유전자 입체 구조가 동적으로 변화하며 세포 운명을 결정하는 과정을 실시간으로 추적하는 데 성공했다.
아울러 연구팀은 실험 과정에서 게놈 3차 구조 정보는 유전자 발현을 조절하는 핵심 인자인 인핸서(Enhancer)와 프로모터(Promoter) 사이의 물리적 접촉을 더 정확하게 규명했다.
이와 함께 기존 단일세포 후성유전체 방식보다 인핸서-유전자 관계를 정의하는 정확도가 훨씬 높다는 사실도 입증했다.
정 교수는 “AI로 데이터 한계를 극복해 유전자 조절 관계를 기존보다 훨씬 정밀하게 찾아낸 것이 이번 연구의 핵심"이라며 ”분석 비용을 획기적으로 낮춰 대규모 분자 지도 구축이 가능해진 만큼, 암, 파킨슨 등 복잡 질환이 시작되는 순간을 포착해 환자 맞춤형 치료 타깃을 발굴할 수 있을 것“이라고 설명했다.
한편, 이번 연구는 KAIST 양동찬 박사가 공동 제1저자로, 김규광 박사가 주요 연구진으로 참여했고, 연구결과는 지난 19일 국제학술지 ‘네이처 바이오테크놀로지(Nature Biotechnology)’에 게재됐다.
(논문명: Trimodal single-cell profiling of transcriptome, epigenome and 3D genome in complex tissues with scHiCAR)











