독도의 혹독한 자연환경에서 살아온 미생물을 난치성 뇌 질환을 치료할 신약 후보 물질로 활용할 수 있다는 연구결과가 나와 주목받고 있다.
한국생명공학연구원(이하 생명연) 화학생물연구센터 장재혁·장준필 박사팀은 한국과학기술연구원(KIST) 천연물시스템생물연구센터 강경수 박사팀과 공동연구로 독도 토양에 서식하는 미생물에서 신경염증을 억제하는 신규 천연물 ‘독도티오신(Dokdothiocin)’을 발견하고 그 작용 가능성을 규명했다.
연구팀이 주목한 대상은 독도 자생식물 땅채송화의 뿌리 주변 토양에서 분리한 방선균 ‘스트렙토마이세스(Streptomyces sp. 20A130)’이다. 스트렙토마이세스는 독도의 강한 해풍과 염분 속에서도 살아남은 미생물이다.
독도는 강한 해풍과 높은 염분, 제한된 토양 환경 등 극한의 자연조건을 가진 화산섬으로, 일반 환경과는 다른 독특한 미생물 군집을 형성해 기존 연구에서 발견되지 않은 새로운 화합물이 존재할 가능성이 높은 지역이다.
연구팀은 이 미생물이 평소 생산하지 않는 새로운 물질을 만들도록 OSMAC(One Strain Many Compounds) 전략을 적용했다.
OSMAC 전략은 하나의 미생물 균주라도 배지 조성, 온도, pH, 배양 형태 등 배양 조건을 변화시켜 서로 다른 대사산물을 생산하는 원리를 토대로 독창적인 새로운 천연물을 발굴할 수 있어 기존 균주로부터 ‘잠재 화학공장’을 여는 방법으로 사용된다.
이를 통해 연구팀은 일반적인 실험 조건에서 발현되지 않던 ‘침묵 유전자(Silent Biosynthetic Gene Cluster)'를 활성화하는 데 성공, 이전에 보고된 적 없는 신규 천연물 ’독도티오신‘을 분리·정제했다.
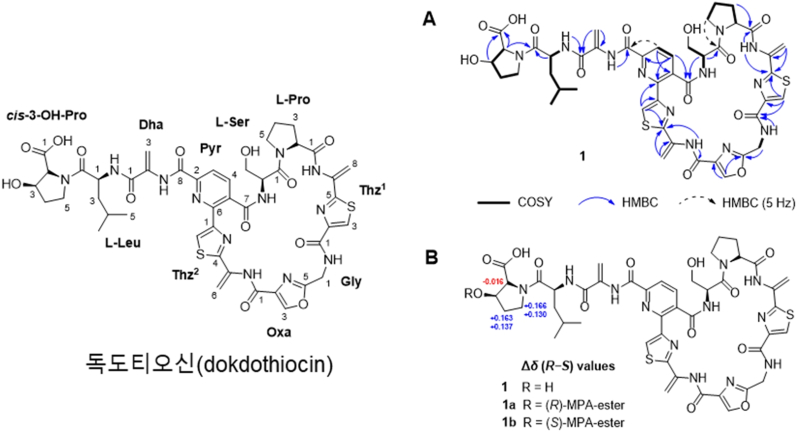
독도티오신은 29개의 원자가 고리 형태로 연결된 매크로사이클 구조를 가진 화합물로, 옥사졸·티아졸·피리딘 등의 이질고리 구조가 복합적으로 배열된 티오펩타이드 계열 물질이다.
특히 기존 티오펩타이드 계열에서 드물게 발견되는 3-하이드록시프롤린(3-hydroxyproline) 잔기를 포함해 구조적 독창성이 높은 것으로 분석됐다.
이 같은 구조적 특징은 기존 치료제와 다른 작용기전을 가질 가능성을 보여주며 차세대 신약 후보 물질로서의 잠재력을 시사한다.
연구팀은 독도티오신의 생리활성을 확인하기 위해 인공지능 기반 분석과 세포 실험을 결합한 연구를 수행했다.
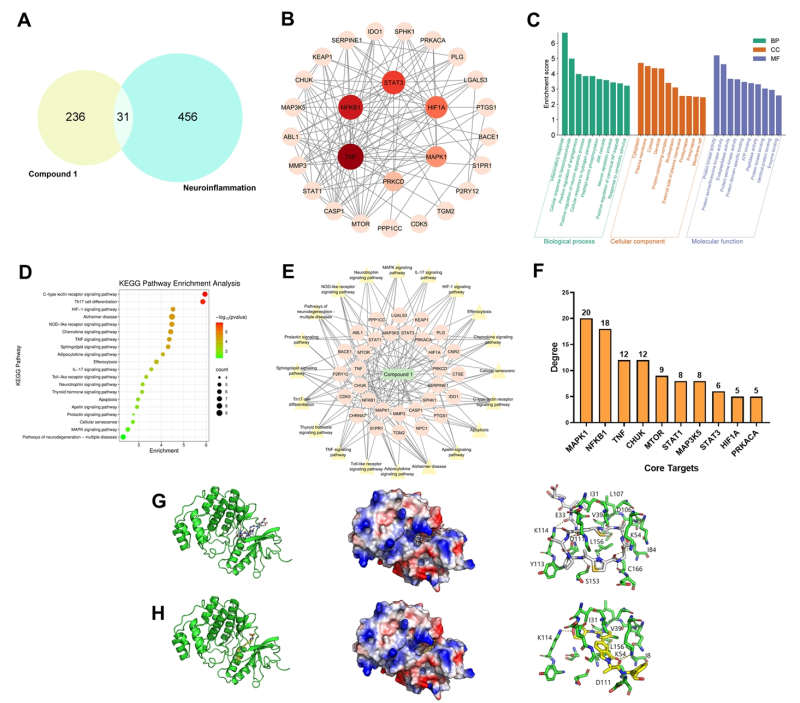
KIST가 개발한 단백질 타깃 예측 인공지능 기술을 활용해 독도티오신이 결합할 가능성이 있는 단백질을 분석한 결과 뇌 염증 반응과 관련된 주요 신호 전달 경로를 조절할 가능성이 있는 것으로 나타났다.
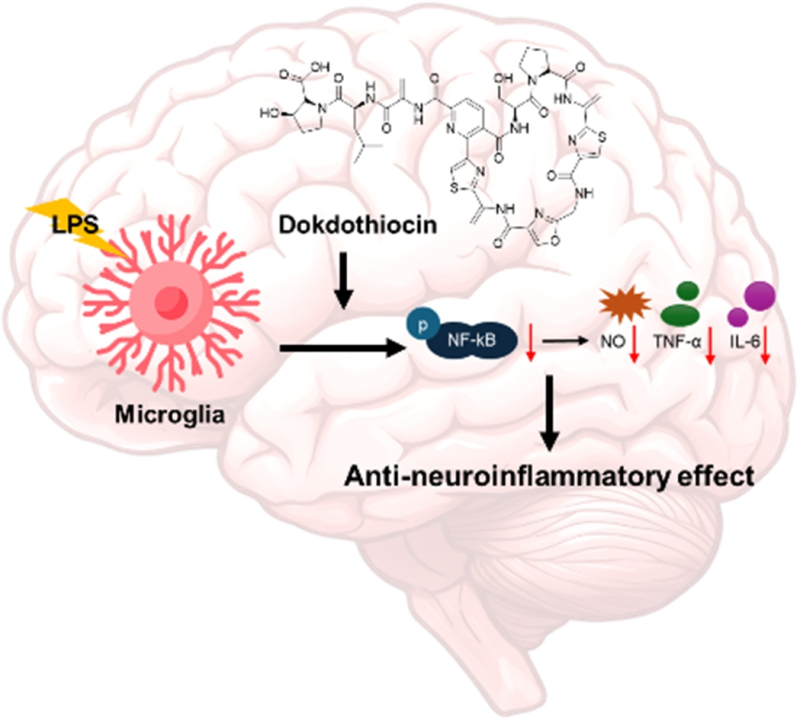
이어 진행된 세포 실험에서 뇌 면역세포 ’미세아교세포(microglia)‘를 활용해 신경염증 억제 효과를 확인했다.
미세아교세포는 뇌와 척수에 존재하는 면역세포로, 과도하게 활성화될 경우 알츠하이머병이나 파킨슨병 같은 퇴행성 뇌 질환의 원인이 되는 신경염증을 유발하는 것으로 알려졌다.
실험 결과 독도티오신은 염증 유도 물질에 의해 증가하는 일산화질소 생성을 억제하고, 염증 반응을 조절하는 NF-κB와 MAPK 등 주요 신호 전달 경로를 차단했다.
아울러 염증성 사이토카인 생성도 감소시키는 효과를 보였다.
이를 인공지능으로 분석한 예측 작용 경로와 실제 실험 결과가 일치해 독도티오신의 신경염증 억제 가능성을 과학적으로 입증했다.
이번 연구는 단순히 새로운 물질을 발견한 것을 넘어 그 물질이 생성되는 생합성 과정과 생리활성 작용 원리까지 규명해 큰 의미를 갖는다.
특히 국내 자연환경에서 확보한 미생물 자원의 과학적 가치와 산업적 활용 가능성을 보여주는 것으로, 연구팀은 그동안 울릉도, 제주도 등의 토양 시료에서 울릉아마이드, 울릉도린, 제주펩틴 등 국내 지역명을 붙인 다양한 신규 천연물을 발굴했다.
연구팀은 향후 독도티오신의 작용 기전과 안전성 검증 연구를 추가로 진행해 신경염증 조절 치료제 개발 가능성을 더욱 구체적으로 확인할 계획이다.
장 박사는 “독도처럼 독특한 자연환경에 서식하는 미생물은 아직 밝혀지지 않은 화학적 다양성을 지닌 중요한 자원”이라며 “이번 연구는 독도 토양 미생물에서 새로운 생리활성 천연물을 발굴하고 그 가능성을 확인한 사례로, 국내 생물자원의 과학적 가치와 신약 개발 잠재력을 보여준 것”이라고 설명했다.
강 박사는 “AI 기반 단백질 타깃 예측 기술을 통해 신물질의 작용 가능 경로를 빠르게 규명했다”며 “앞으로 유전체 분석과 배양 전략, 인공지능 기술을 결합해 숨겨진 생합성 유전자를 체계적으로 탐색하고 새로운 의약 후보물질 발굴 연구를 확대하겠다”고 말했다.
한편, 이번 연구성과는 지난달 27일 국제학술지 'Organic Letters'에 게재됐다.
(논문명: Dokdothiocin, an Anti-Neuroinflammatory Thiopeptide from Streptomyces sp. 20A130 / 교신저자: 생명연 장재혁 박사, 장준필 박사, KIST 강경수 박사 / 제1저자: 생명연 박지훈 석사후연구원, KIST Son Hung Tran 박사과정생))










