한국화학연구원(이하 화학연)이 나노입자와 줄기세포를 결합해 3차원 뼈 조직 재생을 크게 개선하는 기술을 개발했다.
이번 연구는 골절이나 뼈 손상 치료뿐 아니라 차세대 조직재생의학 분야에 중요한 전환점을 제시한다.
화학연 김기영 박사는 선문대 하미진 교수와 공동연구로 인체 지방유래 줄기세포(hADMSC)와 다공성 실리카 나노입자를 결합해 ‘나노 바이오 하이브리드 세포’를 제작, 뼈 형성 능력을 높이는 데 성공했다.
스페로이드, 오가노이드 등 줄기세포를 활용한 3차원 세포 집합체는 장기나 조직을 모사하지만, 내부 영양·산소 공급이 부족해 세포가 죽거나 균일하게 뼈로 분화되지 못하는 문제 때문에 실제 뼈 재생 치료나 약물 평가에 적용하기 어려웠다.
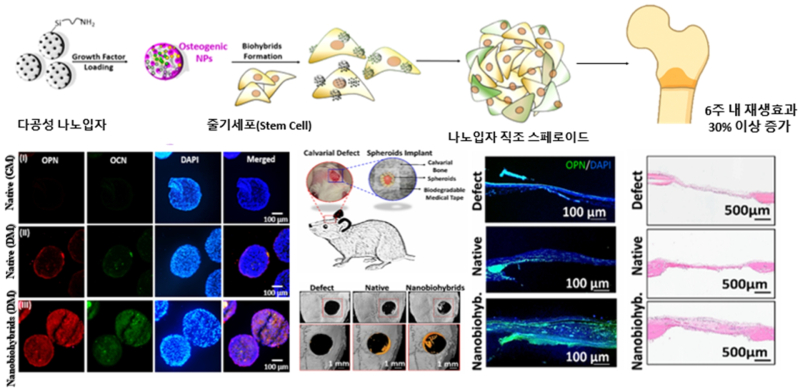
연구팀은 줄기세포 표면에 다공성 실리카 나노입자를 보론-페놀 결합으로 고르게 부착해 세포들이 서로 얽혀 안정적인 구형 구조를 형성하도록 유도함으로써 새로운 세포-나노 융합체인 ‘나노입자-직조 줄기세포’를 제작했다.

나노입자는 줄기세포 사이에서 지지대와 뼈 형성 촉진제 역할을 동시에 한다.
이는 나노입자가 지지체 역할 뿐만 아니라 뼈 형성을 촉진하는 신호물질을 싣고 서서히 방출하며 줄기세포가 원하는 방향으로 균일하게 분화되도록 유도하는 것으로, 영양제 캡슐을 등에 짊어진 세포들이 스스로 뼈로 변신하는 것과 같다.
때문에 골절 환자의 회복 기간을 단축시키고, 고령화 사회에서 증가하는 골다공증·치매성 골손상 치료에 유용하다.
실제 실험에서 나노입자-줄기세포 스페로이드는 기존 방식보다 세포 생존율이 높고, 뼈세포로 균일하게 분화했다.
특히 쥐 두개골 결손 모델에 이식했을 때 6주 만에 결손 부위의 36%가 새 뼈로 채워져 세포만으로 구성된 스페로이드 대비 재생률이 1.3배 높았다.
이번 연구는 향후 대형 동물 모델과 임상연구를 거치면 환자 맞춤형 뼈 이식재 개발에 적용될 전망이다.
김 박사는 “기존 단순 세포 스페로이드 한계를 극복하고 3차원 세포치료제와 조직재생 플랫폼의 새로운 가능성을 높였다”며 “뼈뿐 아니라 연골, 피부 등 다양한 조직재생에도 확장될 수 있다”고 설명했다.
한편, 이번 연구성과는 지난 8월 국제학술지 ‘ACS Biomaterials Science & Engineering(IF : 5.5)’에 게재됐다.











