파킨슨병보다 진행이 빠른 희귀 난치성 뇌질환 ‘다계통 위축증(MSA)’의 발병 원인을 찾았다.
한국연구재단은 서울대 이승재 교수 연구팀이 단백질 ‘톨유사수용체2(TLR2)’가 다계통 위축증 발병의 핵심 통로 역할을 한다는 사실을 규명했다고 27일 밝혔다.
다계통 위축증은 소뇌와 기저핵 신경 세포가 파괴되는 치명적인 질환으로, 증상은 파킨슨병과 비슷하지만 진행 속도가 훨씬 빠르고 발병 후 3~5년 내에 걷기 힘들 정도로 악화된다.
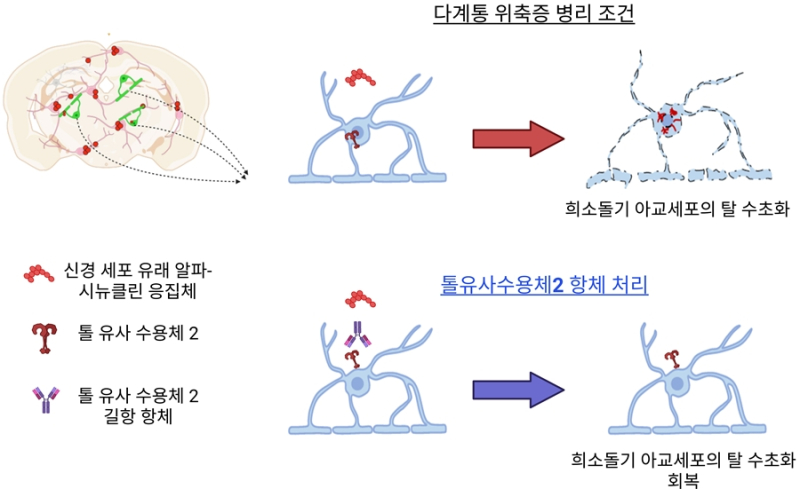
이 병에 걸린 환자의 뇌는 신경세포를 절연체처럼 감싸 전기신호를 빠르게 전달하도록 돕는 ‘희소돌기아교세포’ 안에 비정상 단백질인 ‘알파-시뉴클린’ 덩어리가 쌓인다.
그러나 희소돌기아교세포는 이 단백질을 거의 만들지 않기 때문에 이 덩어리가 어디서 발생하는지 알 수 없었다.
연구팀은 세포에 강제로 단백질을 주입하던 기존 연구방식에서 탈피해 사람 줄기세포로 만든 희소돌기아교세포와 쥐 뇌세포를 이용한 새로운 실험 모델을 만들었다.
이를 활용한 결과 신경세포에서 만들어진 비정상 알파-시뉴클린 덩어리가 희소돌기아교세포 안으로 흡수되는 현상을 확인했다.
아울러 알파-시뉴클린 덩어리가 들어오는 문 역할을 하는 수용체는 면역을 담당하는 단백질 중 하나인 ‘TLR2’임을 규명했다.
실제 다계통 위축증 환자의 뇌 조직 분석 결과 TLR2가 비정상적으로 많이 늘어났다.
희소돌기아교세포가 TLR2를 통해 알파-시뉴클린 덩어리를 흡수하면 신경망을 감싸 보호하는 수초화 과정에 필수적인 유전자 작동이 멈춰 신경망이 망가지는 결과를 초래했다.
원인을 찾은 연구팀은 세포와 동물 모델에 TLR2 기능을 막는 표적 단일클론항체 'NM-101'을 투여함으로써 항체를 이용해 문을 걸어 잠그자 희소돌기아교세포 안에 알파-시뉴클린 단백질이 쌓이는 현상이 크게 줄었다.
이에 작동을 멈췄던 수초화 관련 유전자도 제 기능을 회복했다.
특히 쥐 신경세포 몸통에서 뻗어 나온 줄기인 축삭의 손상과 운동 장애가 좋아졌고, 수명까지 늘어나는 치료 효과를 입증했다.
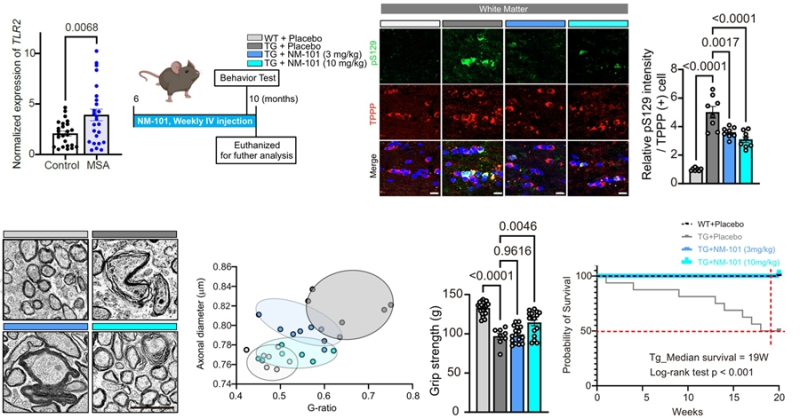
이번 연구는 병리 단백질 자체가 아닌, 이를 매개하는 수용체를 차단함으로써 구조적 이질성이 높은 단백질 응집체의 전이를 억제하는 새로운 치료 패러다임을 제시해 큰 의미를 갖는다.
이 교수는 "모양과 구조가 제각각인 비정상 단백질 자체를 없애려던 기존 항체 치료제 한계를 극복하기 위해 단백질이 이동하는 통로인 수용체를 차단하는 새로운 접근법을 실험으로 증명했다"며 "이 전략은 다계통 위축증뿐만 아니라 파킨슨병 등 공통된 기전을 공유하는 다양한 시뉴클린병증 치료를 위한 범용 플랫폼으로 확장할 수 있을 것"이라고 설명했다.
한편, 이번 연구결과는 지난달 국제학술지 '네이처 커뮤니케이션즈'에 게재됐다.
(논문명: Anti-TLR2 immunotherapy modulates neuron-to-oligodendrocyte propagation of α-synuclein in mouse and human models / 저자 - 이승재 교수(교신저자/서울대 의과대학), 배은진 박사 (제 1 저자/서울대 의과대학), 함상우 박사 (제 1 저자/ 뉴라메디), 정연우 학생 (공동 저자/서울대 의과대학), 양우승 연구원 (공동 저자/뉴라메디), 신지민 연구원 (공동 저자/뉴라메디), 이원재 연구원 (공동 저자/뉴라메디), 안우정 연구원 (공동 저자/건국대), 윤예슬 박사 (공동 저자/건국대), 이혜진 교수 (공동 저자/건국대), 이상환 박사 (공동 저자/서울대 의과대학), 박성혜 교수 (공동 저자/서울대 의과대학))










