KAIST가 구글 딥마인드 '알파폴드 3(AlphaFold 3)' 이상의 성능으로 약물이 단백질에 단순히 결합하는지 여부와 실제 활성까지 판별하는 단백질 구조예측 인공지능(AI)을 개발했다.
KAIST 바이오및뇌공학과 이관수 교수팀은 약물 후보물질이 단백질 활성화까지 예측하는 AI 모델 ‘GPCRact’를 개발했다고 8일 밝혔다.
단백질 구조 예측 분야는 알파폴드가 단백질의 3차원 구조를 예측하며 큰 성과를 거뒀지만, 약물이 단백질에 결합한 뒤 실제로 기능을 활성화하거나 억제하는지 예측하지 못한다.
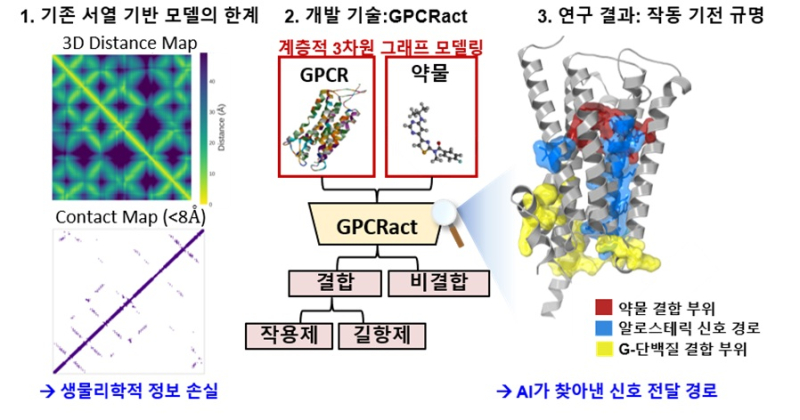
GPCRact는 약물 작용 과정을 결합 단계와 단백질 내부 신호전달 단계로 나눠 AI가 학습하도록 설계한 것이 특징이다.
연구팀은 단백질의 3차원 구조를 원자 수준 그래프로 표현하고 그래프 신경망 기술과 ‘어텐션 메커니즘(attention mechanism)’을 적용해 단백질 내부에서 전달되는 신호 경로를 학습하도록 했다. 이를 통해 AI가 약물 결합 신호와 함께 단백질 내부 신호 전파 과정을 분석해 실제 단백질 활성 여부를 예측할 수 있다.
이 모델은 특히 단순히 활성이나 비활성의 결과만 제시하는 기존 모델과 달리 예측의 근거가 되는 단백질 내부 핵심 신호 경로까지 제시한다. 이를 통해 연구팀은 AI의 의사결정 과정을 설명할 수 있는 해석 가능한 AI를 구현했다.
이 기술을 대표적인 신약 표적인 ‘G-단백질 결합 수용체(GPCR)’에 적용한 결과 약물 후보 물질이 단순히 결합하는지를 넘어 실제 단백질의 기능을 활성화하거나 억제하는지를 예측하는 성능이 기존 모델보다 크게 향상된 것으로 나타났다.
GPCR은 세포막 표면에 존재하는 단백질로 외부에서 전달되는 다양한 신호를 세포 내부로 전달하는 신호 수신기 역할을 하며, 인체에는 800여 종의 GPCR이 존재한다.
현재 시판 중인 의약품의 30~40%가 이를 표적으로 할 만큼 신약 개발에서 가장 중요한 단백질 군 중 하나로, 심장 박동과 혈압 조절, 통증 감지, 면역 반응, 감정 조절 등 다양한 생리 기능에 관여하는 핵심 단백질이다.
그러나 약물이 GPCR에 결합하더라도 실제로 원하는 생리 기능이 작동하지 않는 경우가 많다.
이는 결합 이후 단백질 내부에서 발생하는 알로스테릭 신호 전파 과정이 실제 작용 여부를 결정하기 때문이다.
연구팀이 개발한 GPCRact 모델은 이러한 단백질 내부 신호 전달 경로를 추적해 약물 활성 예측 성능을 크게 향상시켰다.
특히 약물이 결합했을 때 그 신호가 단백질 내부를 거쳐 멀리 떨어진 부위까지 전달되는 ‘알로스테릭’ 신호 경로를 파악해 실제 활성 여부를 정밀하게 예측한다.
이번 연구는 향후 GPCR을 표적으로 하는 다양한 질환 연구에서 약물의 결합 여부뿐 아니라 실제 활성 여부까지 예측하는 정밀 신약 개발 AI 플랫폼으로 활용될 것으로 기대된다.
이 교수는 “이번 연구는 약물이 단백질 한 지점에 결합할 때 생기는 구조 변화가 전체로 퍼져 기능을 조절하는 알로스테릭 원리를 AI로 구현한 것”이라며 “후보 물질이 실제 생체 내에서 작동하는 경로를 원자 수준에서 판별해 신약 개발 성공률을 획기적으로 높일 것”이라고 말했다.
한편 이번 연구는 손효진 박사과정이 제1저자로 참여했고 연구 성과는 지난 1월 국제학술지 `브리핑스 인 바이오인포매틱스(Briefings in Bioinformatics, JCR 상위 2.2%)'에 게재됐다.
(논문명 : GPCRact: a hierarchical framework for predicting ligand-induced GPCR activity via allosteric communication modeling)











